Клас:___________ П.І.:___________________________________
Контрольна робота № 2
9клас
Завдання 1-6 мають по чотири варіанти відповіді.
У кожному завданні лише одна правильна. ( по 0,5б.)
1.Позначте формулу оцтової кислоти:
А. С2Н5ОН. Б. НСООН. В. СН3СООН. Г. С17Н35СООН.
2. Загальна формула насичених одноатомних спиртів:
А. Сп(Н2О)m; Б. R1CООR2; В. СН3СООН; Г. СпН2п +1ОН.
3. Функціональна група карбонових кислот:
А. -ОН; Б . - СООН; В. -СОН; Г. -СОО-
4. Пентан-2-ол – це органічна речовина, що належать до класу:
А. Спиртів. Б. Естерів. В. Карбонових кислот. Г. Вуглеводів.
5. Розчин оцтової кислоти змінює колір лакмусу на:
А. Фіолетовий. Б. Червоний. В. Малиновий. Г. Синій.
6. Етилметаноат належить до класу:
А. Жирів. Б. Естерів. В. Алканів. Г. Спиртів.
Завдання 7 – 9 можуть мати дві і більше правильні відповіді.
7. (1б.) Виберіть властивості, які притаманні гліцерину:
А. Біла кристалічна речовина.
Б. Розчинний у воді.
В. Солодкий на смак.
Г. Волокниста речовина, молекули якої мають лінійну структуру.
8. (1б.) Виберіть галузі застосування оцтової кислоти:
А. Добування глюкози. Б. Виробництво етилового спирту.
В. Продукт харчування. Г. Виготовлення штучних волокон.
9. (1б.) Позначте речовини, з якими може реагувати етиловий спирт:
А. Na2О; Б. СН3СООН; В. СаСО3; Г. О2.
10. (2б.) Закінчити рівняння реакцій:
А. СН3СООН + Nа2СО3 →
Б. С2Н5ОН + К →
В. СН3ОН + О2 →
Г. СН3СООН + С3Н7ОН→
11.(2б.) Здійснити перетворення за схемою:
СН4 → СН3Сl → СН3ОН→ СН3СООСН3
↓
СО2
12. (2б.) Обчисліть об’єм водню, який виділиться при взаємодії магнію
із 800 г оцту, масова частка кислоти в якому становить 6%.
Практична робота №5
Тема: Виявлення органічних сполук у харчових
продуктах
Мета: виявити
органічні продукти в харчових продуктах; продовжити формувати вміння працювати
з хімічним посудом та реактивами;
формувати вміння самостійно виконувати досліди за поясненням у протоколі,
виконувати досліди з дотриманням правил техніки
Зробіть записи в зошіті
ПЕРЕГЛЯНЬТЕ ВІДЕО







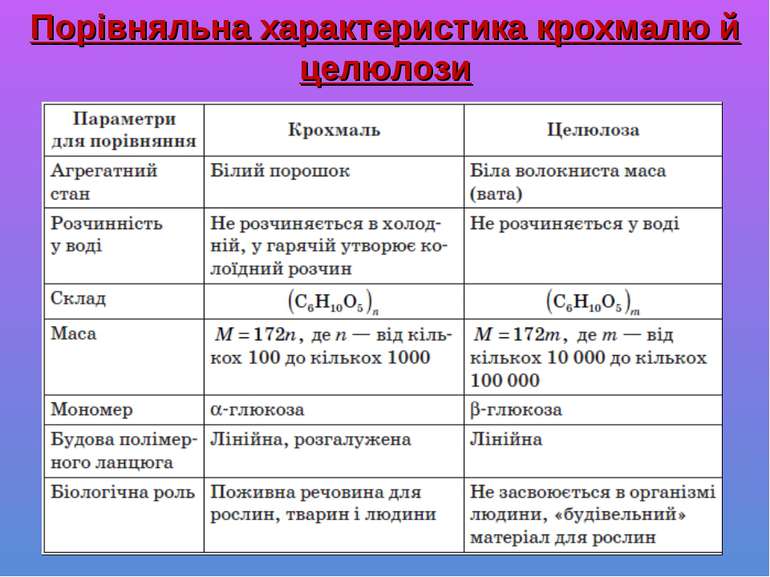
38. Крохмаль і целюлоза.
1. Зробіть запис у зошиті:






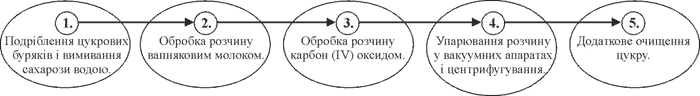
37. Вуглеводи. САХАРОЗА (С12Н22О11)
(ПАРАГРАФ 37, СТОР.180-181)
Фізичні властивості

Хімічні властивості
Схема 16
Добування
Вуглеводи. ГЛЮКОЗА.
(ПАРАГРАФ 37, СТОР.178-180)
Зробіть запис у зошиті:
4.ЯКІСНІ РЕАКЦІЇ НА ГЛЮКОЗУ:
Глюкоза прявляє хімічні властивості характерні для багатоатомних спиртів і альдегідів.
5. Взаємодія глюкози з купрум (II) гідроксидом
6.1. (як багатоатомний спирт):
6.2. (Як альдегід):
1. Зробити конспект.
2. Прочитати (ПАРАГРАФ 37, СТОР.178-180).
3.№146 (стор. 182)
Оновлено 08.04.2020
№
|
Назва досліду
|
спостереження
|
Рівняння реакцій,
висновки
|
1
|
Дія оцтової кислоти на універсальний індикатор
|
Скляною паличкою наносимо краплю кислоти. Індикатор
показав ( яке середовище?)
|
Запис рівняння електролітичної дисоціації
CH3COOH↔
Оцтова кислота – слабкий електроліт, дисоціює, утворюючи гідроген – йони, тому змінює колір
індикаторів.
|
2
|
Взаємодія оцтової кислоти з основами (лугами)
|
У чисту пробірку наливаю 1 мл розчину NaOH, додаю метилоранж, який
набуває ____
забарвлення
Після доливання розчину оцтової кислоти забарвлення _______
|
CH3COOH+NaOH→
Тип цієї реакції ________
Скласти повне та скорочене йонне рівняння
Оцтова кислота реагує з лугами, утворюючи сіль і воду.
|
3
|
Взаємодія оцтової кислоти з металами
|
В пробірку з порошком Mg доливаю 1 мл CH3COOH. Внаслідок
реакції виділяється газ ____________
|
CH3COOH+Mg→
Тип цієї реакції________
Оцтова кислота реагує з
металами, що в ряді напруг стоять до Гідрогену, утворюючи сіль і водень.
|
4
|
Взаємодія оцтової кислоти з основними оксидами
|
В пробірку з білим порошком MgО доливаю 1 мл CH3COOH.
Відбувається розчинення порошку
|
CH3COOH+MgО→
Тип цієї реакції________
Утворюються речовини______
|
5
|
Взаємодія оцтової кислоти з солями
|
В пробірку з розчином CH3COOH.
наливаю 1 мл Na2CO3
Внаслідок реакції виділяється газ ____
|
CH3COOH+ Na2CO3 →
Тип цієї реакції ________
Скласти повне та скорочене йонне рівняння
Оцтова кислота реагує солями,
якщо при цьому утворюється осад, газ або малодисоційована речовина.
|
Подібність властивостей органічних і неорганічних кислот, характеризують такі властивості етанової кислоти:
параграф 27 №105;
параграф 28 №111;
параграф 29 №117;
параграф 30 №4;
параграф 33 №131;
параграф 34 №1-3;








Можно ещё выполнять д/з?
ВідповістиВидалитиНаписано что практическую нужно выполнять по 35 параграфу.Или как правильно?
ВідповістиВидалити